Скрининг за рак на маточната шийка, триаж и диагностични стратегии
HPV ваксиниране
Един от основните методи за превенция при рак на маточната шийка е HPV ваксинирането. Научете повече, като прочетете съответния документ на СЗО относно ваксинацията срещу HPV.
Скрининг за рак на маточната шийка: какви възможности съществуват
HPV ДНК тест: валидиран за първичен скрининг1
HPV ДНК скринингът идентифицира жени с риск от рак на маточната шийка с по-голяма чувствителност, спрямо PAP цитологичен скрининг само. Скринингът с cobas®HPV тест не само открива в по-висок процент високостепенно заболяване, спрямо PAP тест използван самостоятелно, но също така подпомага ефективността на скрининга. Едновременните резултати 3-в-1 за HPV 16, HPV 18 и останалите 12 високорискови генотипи позволяват стратификация на HPV риска като подобрение, спрямо по-високата специфичност за PAP цитологията.
PAP цитология
От въвеждането си през 40-те години на миналия век изследването на PAP допринася за намаляване на рака на маточната шийка с приблизително 70% чрез откриване на клетъчни аномалии2. Въпреки това, поради ниската чувствителност на PAP да открива предракови цервикални лезии3, поради силно вариращите понякога резултати при интерпретацията в различните лаборатории4 и поради ниската откриваемост на аденокарцином5, той има значителни ограничения като дългосрочно, глобално решение да идентифицира жените с риск от цервикална болест6.
HPV co-testing – първичен скрининг с PAP цитология и HPV тест
За да се подобри ниската чувствителност на PAP цитологията, използвана самостоятелно за скрининг на рак на маточната шийка, HPV съвместното тестване (co-testing) е опция, която разчита на PAP цитологията заедно с HPV тестване. Докато тази практика се оказва по-добра при откриване на предракови и ракови заболявания на шийката на матката6, тя е само незначително по-добра от самостоятелния скрининг на HPV и е неефективна от гледна точка на разходите за страните с ограничени ресурси. Когато информацията за HPV генотипиране е включена като част от резултата от теста за HPV, жените могат да бъдат допълнително стратифицирани на база на риска. Една на всеки 10 жени, положителни за HPV 16 и / или HPV 18, има високостепенно заболяване, което се пропуска, ако е тествана само с цитология7.
Опции за триаж за необичайни резултати от скрининга
Биомаркер или PAP цитология
Алгоритмите за първичен скрининг на HPV често включват PAP цитология като подходящ метод за триаж. Тестовете от следващо поколение, които разчитат на двуцветна биомаркерна технология, предлагат значителни предимства пред този традиционен подход. Вместо да търсят клетъчни промени, които са морфологични и могат да бъдат пропуснати поради тяхната субективност, резултатите, базирани на едновременната експресия на p16 и Ki-67 в една клетка, демонстрират по-категорично и обективно, че HPV инфекцията показва признаци на онкогенна трансформация.
CINtec® PLUS Cytology е одобрен от FDA, CE-IVD обективен тест за биомаркери с двойно оцветяване за p16 и Ki-67. Може да бъде използван за триаж на положителни резултати от първичен скрининг на HPV и помага при вече идентифицирани случаи на несъответствие в резултата при съвместно (co-testing) тестване (HPV положителен/PAP цитология нормална), ASC-US цитология (атипични плоскоклетъчни клетки с неопределено значение) или LSIL (нискостепенно сквамозно интраепителиално увреждане). Ако p16 и Ki-67 бъдат експресирани едновременно в една и съща клетка, това означава наличие на трансформираща се HPV инфекция. Получената информация помага на медицинските специалисти да бъдат сигурни, че препоръчват проследяване само за тези пациенти, които биха имали най-голяма полза от това.
CINtec® PLUS Cytology е първият одобрен биомаркерен тест за триаж, който използва технология с двойно оцветяване за едновременно откриване на p16 и Ki-67, за да осигури силен индикатор за наличието на трансформиращи се HPV инфекции.
Генотипиране на HPV
В някои страни може да се използва генотипиране на HPV за триаж на резултатите от PAP цитология или съвместно тестване. Информацията за генотипиране на HPV допълнително стратифицира риска на жената, за да помогне при насочване на решения за последваща грижа.
Генотипи HPV 16 и HPV 18 приблизително представляват 70% от всички случаи на рак на маточната шийка. Фокусът върху тези генотипи дава на медицинските специалисти полезни детайли в подкрепа на решенията им при лечение. HPV генотип 16 създава по-висок риск от предракови лезии и рак на маточната шийка в сравнение с други генотипи, докато HPV генотип 18 се открива в 57% от случаите, свързани с аденокарцином на шийката на матката. Атипичните жлезисти клетки, предшественикът на аденокарцином на шийката на матката, са по-трудни за откриване с PAP цитология8.
Стратегии за триаж
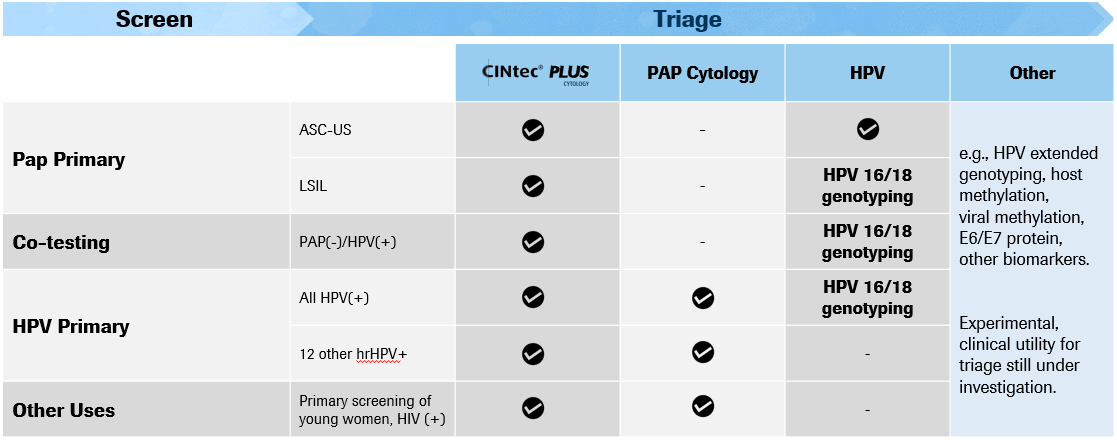
Диагностични стратегии при рак на маточната шийка: какви са възможностите
Оцветяване с хематоксилин и еозин (H&E)
Анализът на цервикални биопсии, използващ H&E или само морфологична интерпретация, може да доведе до фалшиво-отрицателни и фалшиво-положителни резултати, които биха могли да доведат до пропуск в диагностициране на заболяването или ненужно насочване към ексцизионни процедури.
H&E + p16 имунохистохимично (IHC) оцветяване: препоръчителна стратегия9
Допълнителната интерпретация на р16 имунохистохимично оцветяване, заедно с H&E, увеличава диагностичното съответствие на патологичния отговор. Тестът CINtec®Histology е единственият р16 биомаркер, разрешен от FDA и одобрен за клинична/IVD употреба при оценката на проби от цервикална биопсия. Използването на CINtec® Histology от страна на експертите позволява да се идентифицират с 23,8% повече случаи на високостепенно заболяване на маточната шийка в сравнение със самостоятелното използване на H&E (хематоксилин и еозин).
Колпоскопия
Колпоскопията се прави в случаи, че резултатите от скринингa на рак на маточната шийка или тестове за триаж показват абнормни промени в клетките на шийката на матката или ако жената има положителен тест за един от най-високорисковите генотипи – генотип HPV 16 или HPV 18. По препоръка на ASCCP (Американско дружество по колпоскопия и цервикална патология), ASCP (Американско дружество за клинична патология) и ACS (Американско онкологично дружество) жени с нормална цитология, които са позитивни за високорискови HPV 16 или HPV 18, следва да бъдат насочени за незабавна колпоскопия.
Възможно е по време на колпоскопия да се извърши биопсия за вземане на проби от тъкани от области, които изглеждат суспектни. Диагностичната информация, получена от биопсията на маточната шийка, помага да се направи оценка и вземат решения за следващите стъпки. Тези проби се изпращат за лабораторен анализ от патолог за откриване на прекурсори на рак на маточната шийка.
Референции:
- Wright TC, et al. Primary cervical cancer screening with human papillomavirus: end of study results from the ATHENA study using HPV as the first-line screening test. Gynecol Oncol. 2015;136(2):189-97.
- Solomon D, et al. Cervical cancer screening rates in the United States and the potential impact of implementation of screening guidelines. CA Cancer J Clin. 2007;57(2):105-11.
- Whitlock EP, et al. Liquid-based cytology and human papillomavirus testing to screen for cervical cancer: a systematic review for the U.S. Preventive Services Task Force. Ann Intern Med. 2011;155(10):687-97, w214-5.
- Stoler MH, et al. Interobserver reproducibility of cervical cytologic and histologic interpretations: realistic estimates from the ASCUS-LSIL Triage Study. Jama. 2001;285(11):1500-5.
- Herzog TJ, et al. Reducing the burden of glandular carcinomas of the uterine cervix. Am J Obstet Gynecol. 2007;197(6):566-71.
- Isidean SD, et al. Changes on the horizon for cervical cancer screening. Prev Med. 2017;98:1-2.
- Castle PE, Stoler MH, Wright TC Jr, Sharma A, Wright TL, Behrens CM. Performance of carcinogenic human papillomavirus (HPV) testing and HPV16 or HPV18 genotyping for cervical cancer screening of women aged 25 years and older: a subanalysis of the ATHENA study [published online August 23, 2011]. Lancet Oncol. doi:10.1016/S1470-2045(11)70188- 7.
- Ault KA, Joura EA, Kjær SK, et al. Adenocarcinoma in situ and associated human papillomavirus type distribution observed in two clinical trials of a quadrivalent human papillomavirus vaccine. Int J Cancer. 2011;128(6):1344-1353.
- Khan MJ, Castle PE, Lorincz AT, et al. The elevated 10-year risk of cervical precancer and cancer in women with human papillomavirus (HPV) type 16 or 18 and the possible utility of type-specific HPV testing in clinical practice. J Natl Cancer Inst. 2005;97(14):1072-1079.